酵母文库构建验证
小肽团队构建的随机肽库是一种文库构建容量很大的库,可以用来筛选短肽和蛋白质。需要注意的是,随机肽库不受物种限制。通过该平台,研究人员可以筛选与其目标蛋白相互作用的短肽。因此,它是一个非常有用的筛选蛋白质相互作用肽的平台。这种体内筛选方法也非常可行。筛选出的蛋白质还可以再次用于酵母双杂交实验,并结合生物信息学分析,找到与目标蛋白关键结合位点的信息。我们的随机肽库最终在pGADT7GW中构建,并经过Gateway BP-LR反应。
同时,为了进一步测试随机肽库的容量和特性,我们以二级质粒库为模板,设计引物扩增随机肽库序列。将得到的PCR产物用于Illumina测序文库构建。经Illumina Novaseq 6000平台测序后,获得60 bp的reads,用于估算文库容量。结果部分显示,我们的随机肽库构建良好,文库容量足以进行筛选。因此,我们可以宣布我们的随机肽库构建成功。
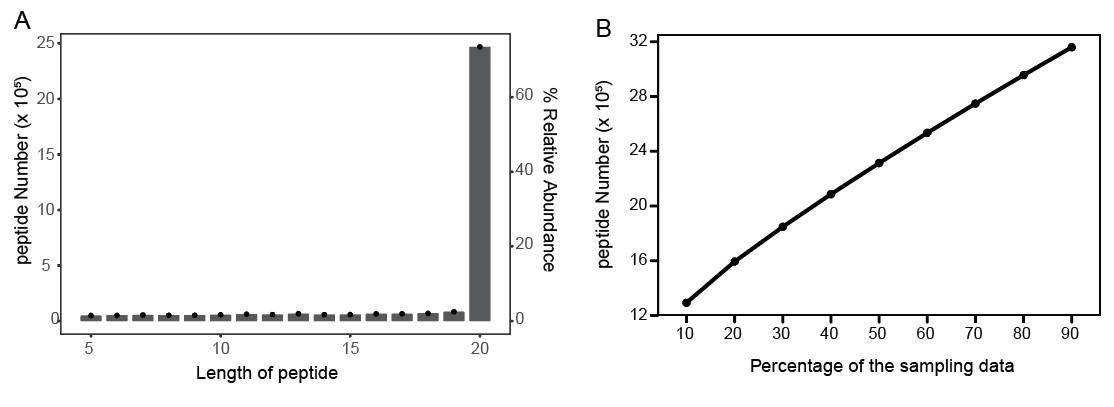
图 2-6 测序结果
通过分子生物学手段在植物中进行验证,构建小肽基因的突变体库,对小肽合成基因缺失突变体,过表达突变体以及小肽受体突变体进行试验,验证小肽的功能以及遗传学稳定性。通过表达对小肽进行人工设计,使其功能发生改变。
“肽强”RegBoost系列小肽产品在再生功能上的验证
“肽强”C25和C26增强不定芽再生
以“肽强”系列小肽肽强C25和肽强C26为例,我们来探究其对植物不定发再生能力的效果。通过不定芽计数的方法得出效果统计图,对筛选出的有显著促进效果的小肽进行遗传学实验。
对肽强C25及肽强C26进行外施试验,实验结果显示肽强C25和肽强C26多肽可以促进不定芽再生。外施10 nM和100 nM 肽强C25和肽强C26多肽后不定芽数目与对照组相比无差别;浓度为1 μM时,肽强C25和肽强C26均可显著促进不定芽再生,并且随着浓度升高促进效应越强(图2-7)说明肽强C25和肽强C26可以显著促进不定芽再生。
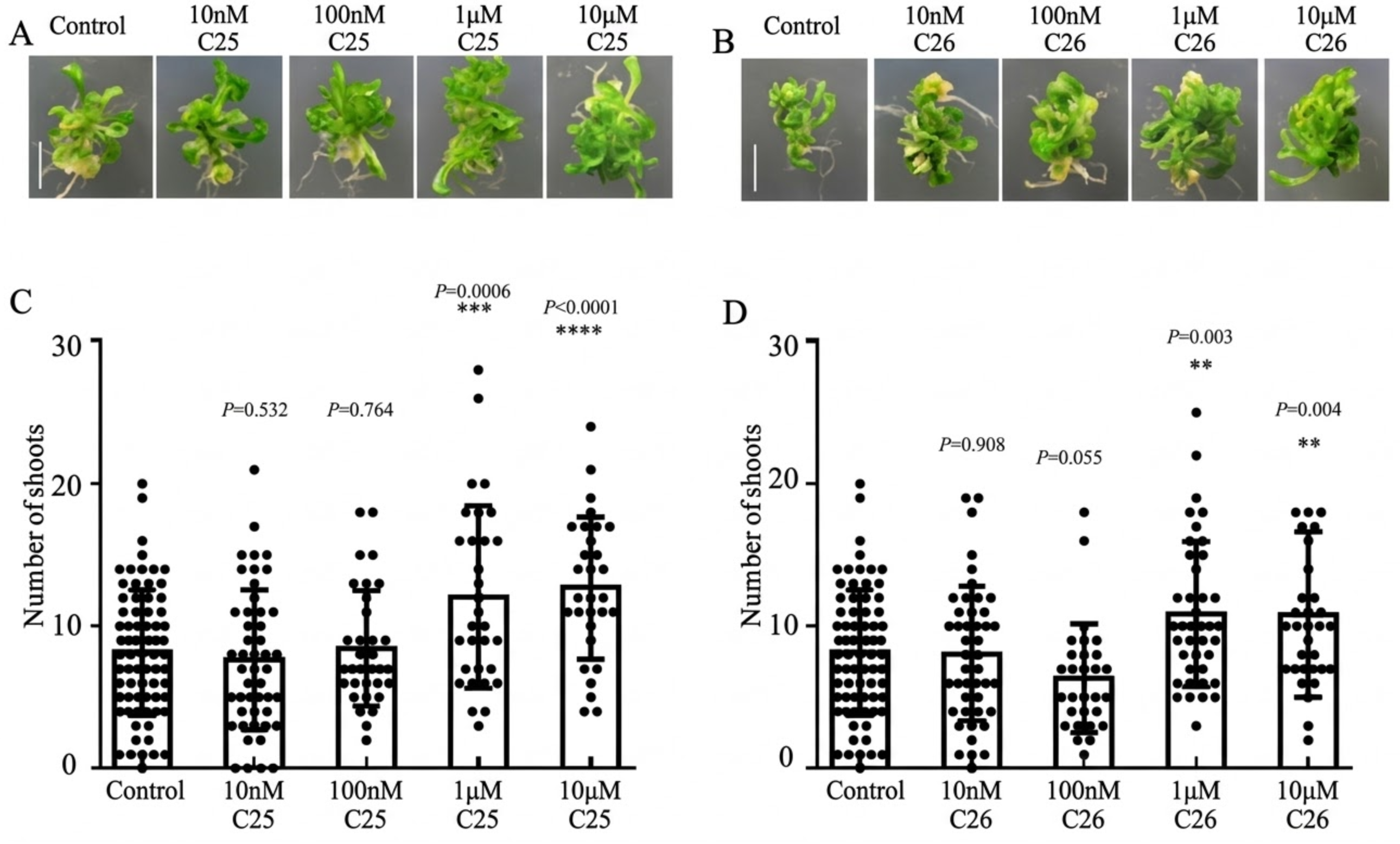
图 2-7 肽强C25/26多肽促进植物芽再生
(图注:A表示外施不同浓度肽强C25多肽植物芽再生典型图,比例尺0.5 cm;B表示外施不同浓度肽强C26多肽植物芽再生典型图,比例尺0.5 cm;C表示在外施不同浓度肽强C25多肽植物芽再生数目统计图;D表示外施不同浓度肽强C26多肽植物芽再生数目统计图;统计数据用平均值±标准误表示,t检验处理组与对照组之间显著性差异。实验重复3次,每次重复样本量N≥24。)
C25和C26基因参与调控植物芽再生
分析了C25功能获得突变体以及C25/26功能缺失突变体在芽再生中的表型。首先我们分析C25功能获得突变体pC25pro:C25:C25t表型,该构建依赖C25自身启动子控制下表达C25基因。我们在此聚焦对pC25pro:C25:C25t过表达转基因株系的表型分析。对过表达株系pC25pro:C25:C25t进行表型分析发现,类似于外施C25多肽,过表达C25导致植物芽再生数目显著增加(图2-9 A-B)。C25-OE(1-4)表示4个pC25pro:C25:C25t转基因纯合株系,类似外施C25多肽。其中C25-OE1和C25-OE2芽再生数目较野生型(8.026±0.356)多分别为:11.640±0.625和9.471±0.814,可能由于超表达株系之间表达量存在差异,因此芽再生数目也存在差异(图2-9 A-B)。
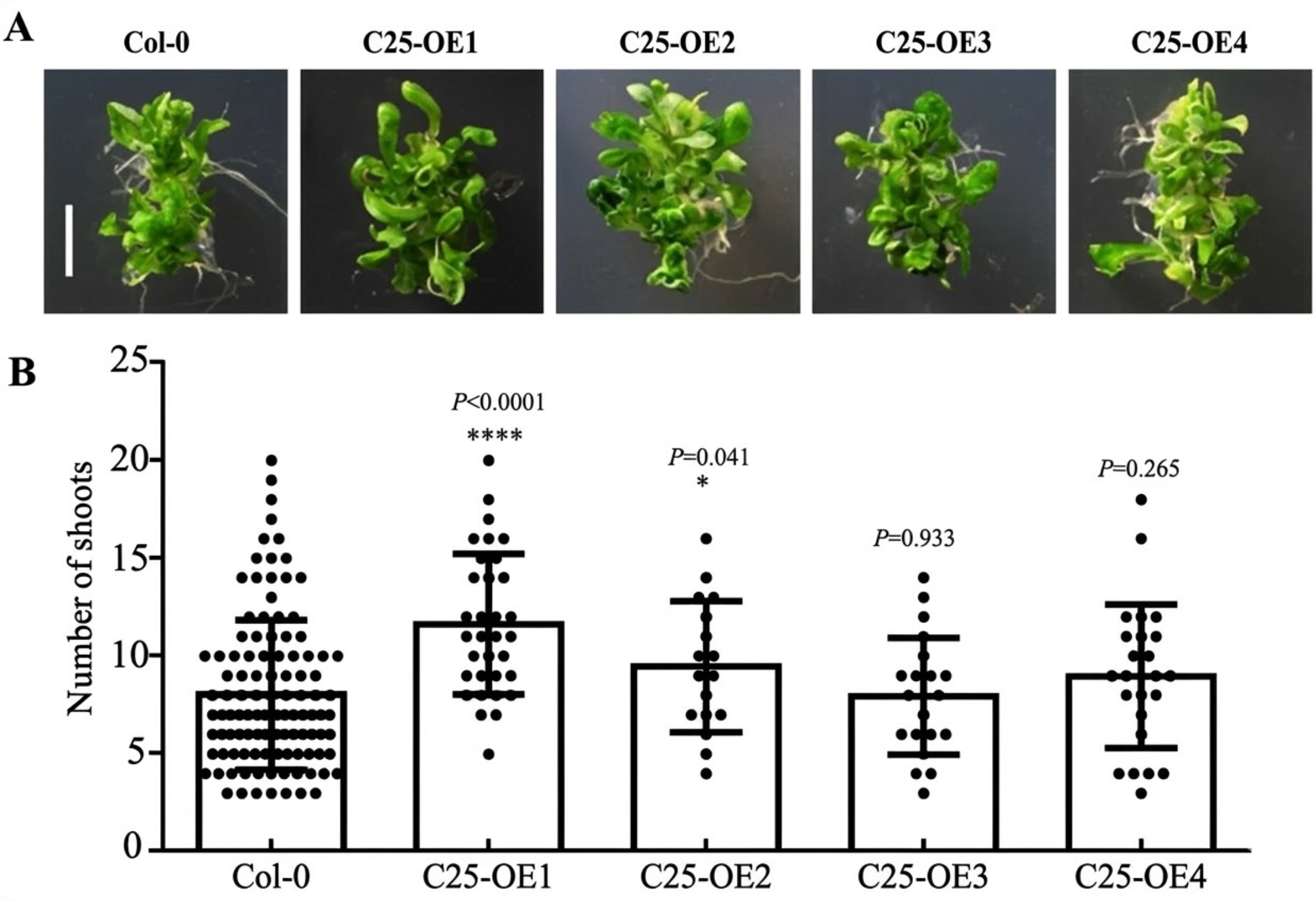
图 2-8 过表达C25造成植物芽再生数目增加
(图注:A表示植物野生型和C25过表达植株芽再生的典型图,比例尺0.5
cm;B表示植物野生型和C25过表达植株芽再生数目统计图。C25-OE(1-4)表示4个pC25pro:C25:C25t转基因纯合株系。统计数据用平均值±标准误表示,t检验处理组与对照组之间显著性差异,*表示0.01
为了进一步确定C25和C26在植物芽再生中的作用,借助CRISPR/Cas9技术获得了C25功能缺失突变体c25-cr1和c25-crp1、C26功能缺失突变体c26-cr1、c26-crp1和c26-crp2;同时也获得了c25
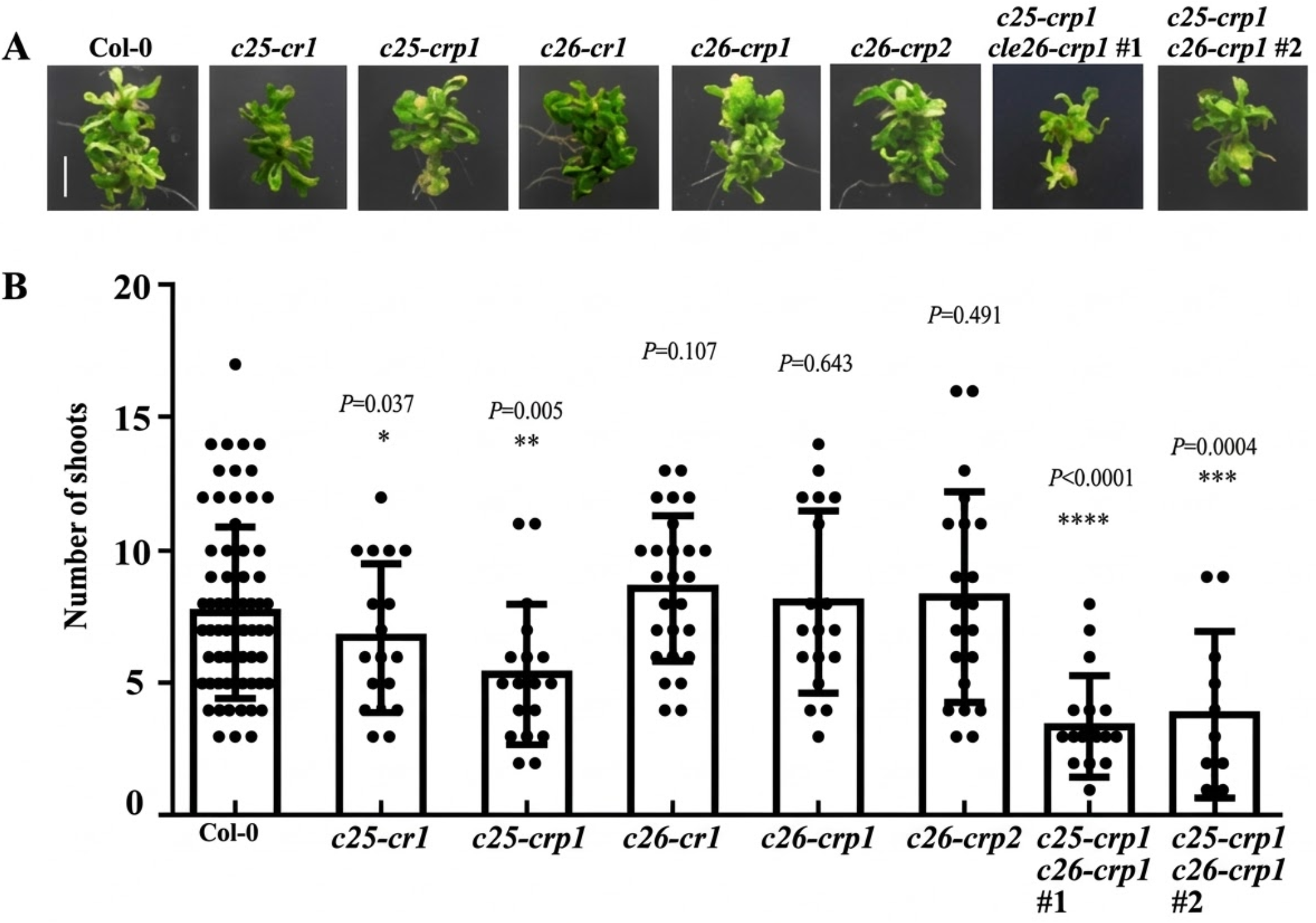
c26双突变体。 为了分析C25/26在芽再生中的功能,利用上述突变体,我们对它们的表型进行分析。在植物芽再生体系下,c25-cr1、c25-crp1突变体芽再生数目(6.747±0.896、5.252±0.505)以及c25
c26双突变体芽数目(3.336±0.604、3.917±0.699)与野生型(7.830±0.390)相比明显减少,但c26-cr1、c26-crp1、c26-crp2突变体芽数目(8.609±0.918、8.073±0.771、8.150±1.349)与野生型无显著差别(图2-10
A-B)。c25
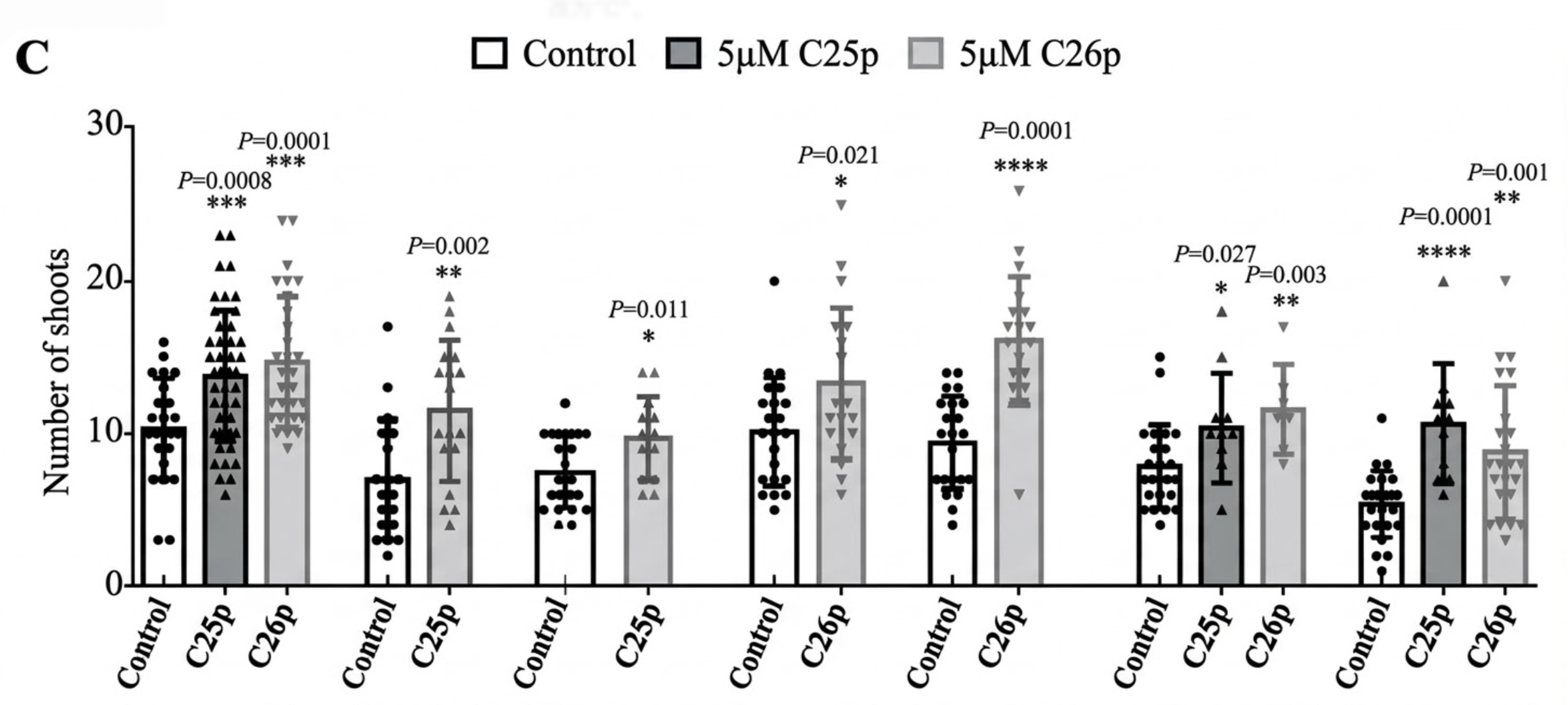
c26双突变体比c25-cr1、c25-crp1突变体芽再生数目少,但差异较小。以上实验结果说明C25多肽可能在促进植物芽再生过程中发挥主要作用,而C26多肽促进作用较微弱。外施5 μM
肽强C25和肽强C26多肽处理C25/26功能缺失突变体发现C25/26功能缺失突变体芽再生数目均表现出明显增加,外施肽强C25和肽强C26多肽可以显著恢复突变体表型(图2-10
C),进一步证明了C25和C26调控植物芽再生。
图2-9 C25和C26功能缺失突变体芽再生的表型
(图注:A表示野生型和C25/26功能缺失突变体芽再生典型图,比例尺0.5 cm;B表示野生型和C25/26功能缺失突变体芽再生数目统计图;C表示外施5 μM
C25和C26野生型和C25/26功能缺失突变体芽再生数目统计图;统计数据用平均值±标准误表示,t检验处理组与对照组之间显著性差异,*表示0.01
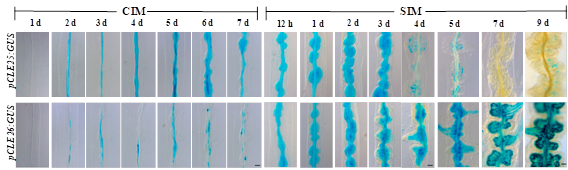
为了进一步明确C25/26在芽再生中的功能,下一步我们对C25和C26的表达情况进行分析。 我们首先使用C25和C26启动子融合报告基因pC25:GUS和pC26:GUS分析C25和C26在芽再生过程中表达情况。如图2-9所示,将外植体移到CIM培养2
d开始C25和C26在愈伤组织表达,猜测C25和C26可能受到外植体伤信号和/或CIM中激素的诱导表达。CIM培养期间,C25在愈伤组织上均匀表达,而C26主要集中在维管组织附近表达。将外植体移到SIM上培养后,C25主要在芽诱导早期表达(芽再生四个阶段中的第一阶段和第二阶段,此时期WUS刚开始表达但尚未出现干细胞龛重建);而C26的表达范围逐渐从维管组织附近向外扩大到愈伤组织凸起,说明C26可能受到SIM中激素的强烈诱导。SIM上培养4
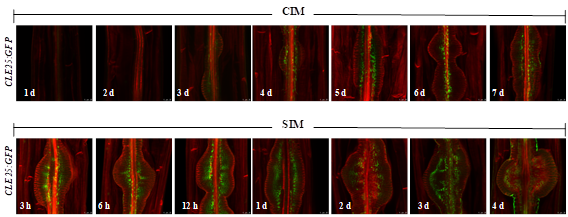
d开始,C25表达逐渐减弱,而C26在整个SIM培养时期持续表达。芽开始形成后C25表达几近消失,而C26表达却很强烈。 为了更清楚研究C25在芽再生过程中的表达,我们利用pC25:SV40-3×GFP:terC25转基因株系,通过激光共聚焦显微镜观察分析C25在植物芽再生过程中的表达(图2-12)。CIM培养2
d C25开始在愈伤组织表达,并且在愈伤组织形成过程中均有表达。将外植体移到SIM上,C25在芽诱导早期部分快速分裂细胞中表达,SIM上4
d其表达逐渐减弱,这些数据与pC25:GUS株系类似(图2-11)。这些结果表明C25多肽促进植物芽再生作用可能主要在芽再生早期(第一阶段和第二阶段)发挥作用,而这两个阶段主要是芽祖细胞发生(WUS标记芽祖细胞属性)。同时,C25在第三阶段和第四阶段(后续WUS调控SAM形成)几乎没有表达,进一步说明C25可能仅仅在WUS介导的芽祖细胞属性获得中发挥功能,而并不在WUS介导的SAM形成中发挥作用。
图2-10 C25(上)和C26(下)在芽再生过程中的表达(比例尺50 μm)
图2-11 C25在芽再生过程中的表达(比例尺25 μm) 多肽一般从分泌细胞产生并运输到靶细胞后被相应的膜受体蛋白识别形成配体-受体复合体,然后导致信号传递引起细胞内一系列生理和生化变化从而发挥其功能。因此,确认C25/26多肽调控植物芽再生过程中的受体是研究C25/26多肽调控植物芽再生信号通路中核心的一步。
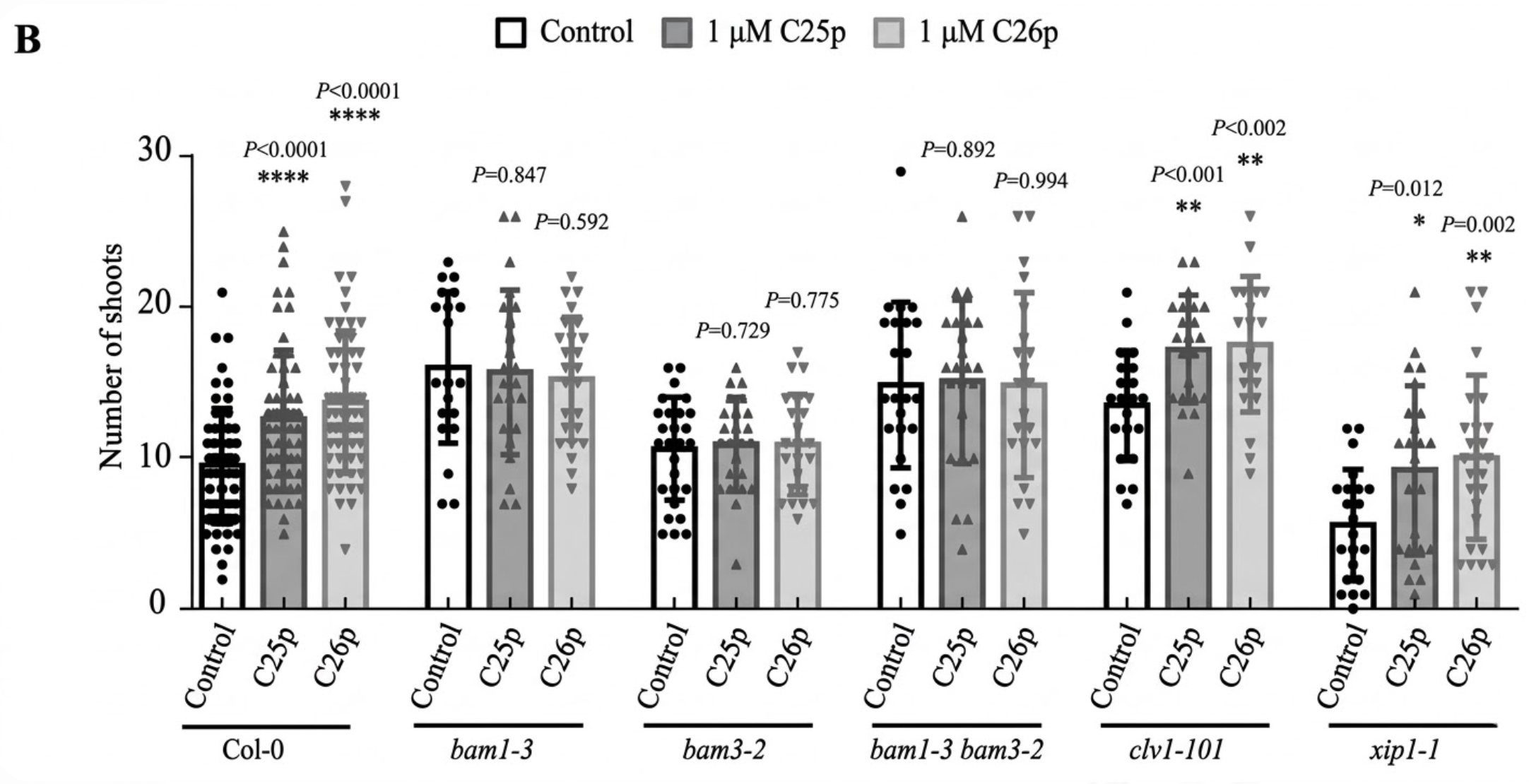
我们首先观察了靶向受体的突变体芽再生数目。实验发现靶向受体作物芽再生数目(16.000±1.087)和靶向受体作物芽再生数目(14.870±1.146)明显比野生型(9.525±0.491)多,而靶向受体作物(10.640±0.644)则与野生型芽再生数目接近(图2-13
A-B)。外施1 µM
C25和C26多肽处理野生型和上述突变体下胚轴外植体,结果显示C25和C26多肽处理野生型外植体芽数目分别为:12.630±0.593和13.730±0.598,较未处理野生型外植体芽再生数目明显增加,而C25和C26多肽处理靶向受体作物突变体芽再生数目为15.700±1.134和15.285±0.813,C25和C26多肽处理靶向受体作物突变体芽再生数目为10.961±0.624和10.917±0.682,C25和C26多肽处理靶向受体作物突变体芽再生数目为15.090±1.121和14.860±1.331,C25和C26多肽处理靶向受体作物突变体芽再生数目则没有显著变化。总而言之,以上实验结果表明该受体可能是C25和C26多肽促进植物芽再生通路中的受体。为了进一步确定C25/26受体,我们同时选取其他功能已知且和家族进化关系非常相近的CLV1和XIP1(CEPR1)进行研究。
图2-12 C25/26多肽调控植物芽再生的受体验证
(图注:A表示外施C25/26多肽野生型、受体相关突变体、clv1-101突变体和xip1-1突变体芽再生典型图,比例尺0.5
cm;B表示外施C25/26多肽野生型、相关突变体、clv1-101突变体和xip1-1突变体芽再生数目统计图;统计数据用平均值±标准误表示,t检验处理组与对照组之间显著性差异,*表示0.01
实验结果发现clv1-101突变体芽再生数目(13.520±0.791)比野生型(9.525±0.491)多,而xip1-1突变体芽再生数目(5.591±0.785)比野生型少,外施C25多肽两个突变体芽再生数目为:17.230±0.764和9.250±1.138,外施C26多肽两个突变体芽再生数目为:17.573±0.977和10.080±1.067,外施C25和C26多肽两个突变体芽再生数目和野生型一样呈现对多肽的响应造成芽数目增加,说明CLV1和XIP1(CEPR1)功能缺失并不影响C25和C26多肽促进植物芽再生,从而间接说明该靶向受体是C25/26介导芽再生过程中的受体。同时,基于clv1芽再生数目显著增加而xip1-1芽再生数目显著减少,我们猜测CLV1和XIP1(CEPR1)可能参与了其他未知多肽介导的芽再生途径。
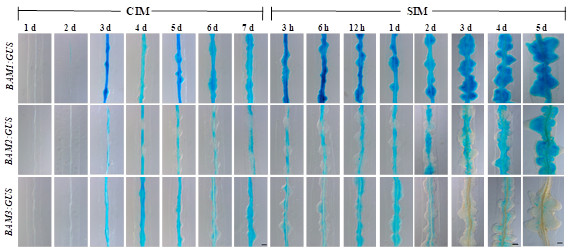
BAM亚家族包括BAM1-3共三个基因,为了研究BAM1-3在芽再生过程中的表达谱,我们利用pBAM1:GUS、pBAM2:GUS和pBAM3:GUS转基因植株进行GUS染色分析BAM1、BAM2和BAM3在植物芽再生过程中表达模式。我们发现BAM1从将外植体移到CIM培养2
d开始在愈伤组织表达,在SIM诱导芽再生的整个过程中都有表达并且其表达模式和C25的表达模式相似(图2-14)。BAM2几乎不在愈伤组织上表达,主要在未形成愈伤组织附近的维管上表达,在芽形成后期开始有表达(图2-14)。
BAM3从将外植体移到CIM培养2
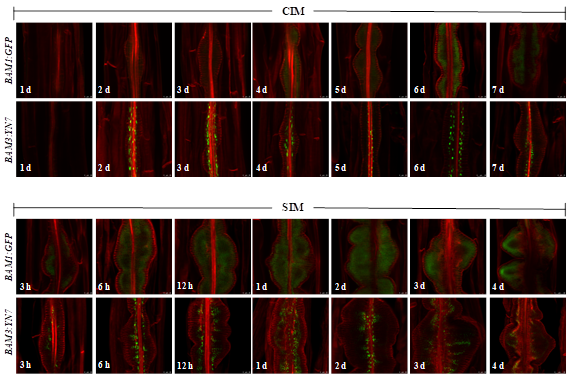
d开始在愈伤组织表达,但表达主要集中在维管组织附近(图11)。为了更清晰地分析BAM1和BAM3的表达模式,我们利用BAM1:GFP和BAM3:YN7转基因株系,通过激光共聚焦显微镜观察在芽再生过程中BAM1和BAM3的表达。BAM1在植物芽再生过程中的表达与GUS染色结果一致,从CIM诱导愈伤组织2
d开始在愈伤组织上表达,在愈伤组织和芽再生过程中都有表达。BAM3从CIM诱导愈伤组织2
d开始表达,主要在维管附近表达。移至SIM上开始BAM3表达范围逐渐扩大至凸起(部分分裂的细胞)。结合上述遗传学结果和基因表达结果,我们确认BAM1/BAM3作为受体参与了C25和C26多肽促进植物芽再生。
图2-13 BAM1, BAM2和BAM3在芽再生过程中的表达(比例尺50 μm)
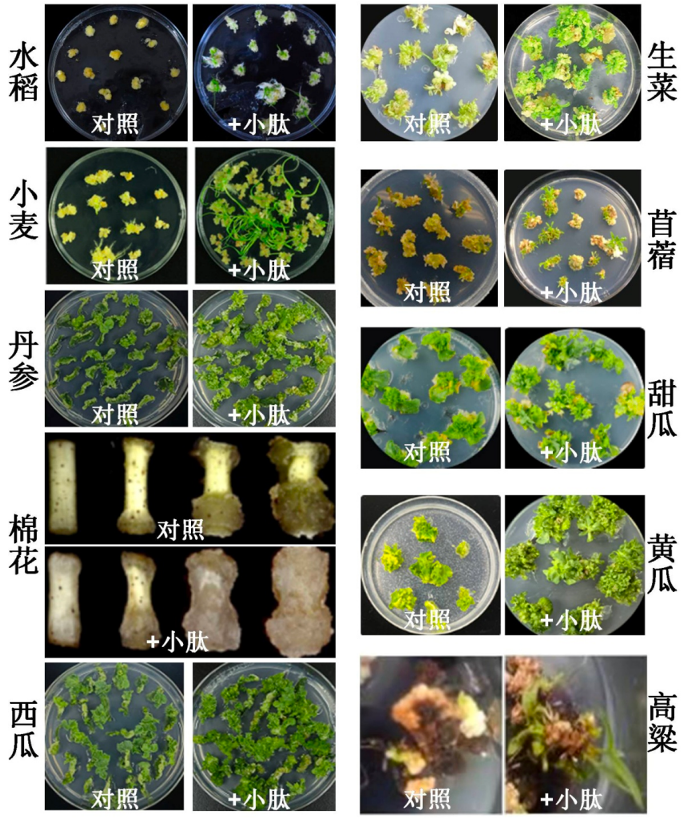
图2-14 BAM1和BAM3在芽再生过程中的表达(比例尺25 μm) 为了验证miPEP是否保守,具有多种作物的广谱效应,我们选择调取多肽处理烟草、番茄、绿豆、黄瓜等常见作物以及人参药材作物中进行外施测试,结果表明适宜浓度的小肽均有促进植株愈伤组织生长以及不定芽和不定根增多的效果(见图2-16)。
图2-15 小肽促进多种作物再生效果图
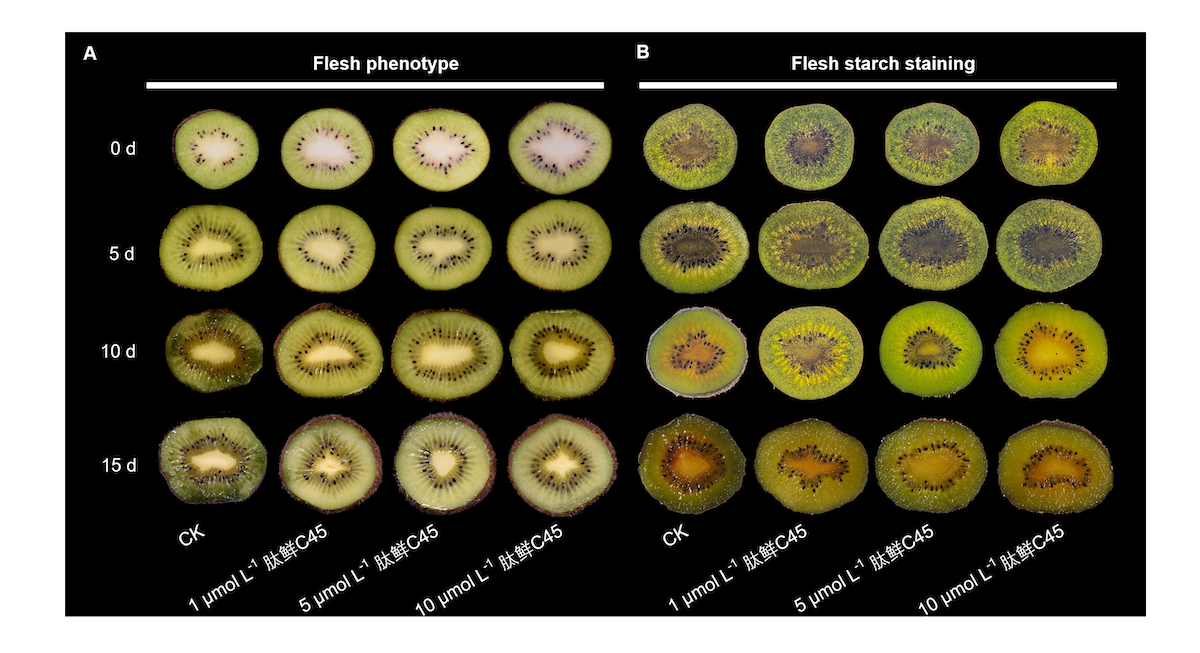
(图注:A-E分别为烟草不定芽、番茄不定根、绿豆不定根、黄瓜不定根和人参不定根的对照和小肽处理的表型。) 本团队通过外源浸泡施用肽鲜C45,建立了针对“徐香”猕猴桃的采后处理工艺。在货架期间,CK组(空白组)果实的果肉组织经历了后熟和衰老,到第10天出现明显的劣变。外源肽鲜C45处理保持了果肉的完整性,直到第15天也未观察到可见的劣变症状。此外,果肉淀粉染色显示,在整个货架期间淀粉逐渐降解,这是衰老的关键指标。CK组果实在第10天几乎不着色(意味着衰老正在进行),而5
µmol L⁻¹肽鲜C45处理显示出明显更强的染色,尤其是在核心区域。
图2-16 肽鲜C45施加后猕猴桃果实形态变化
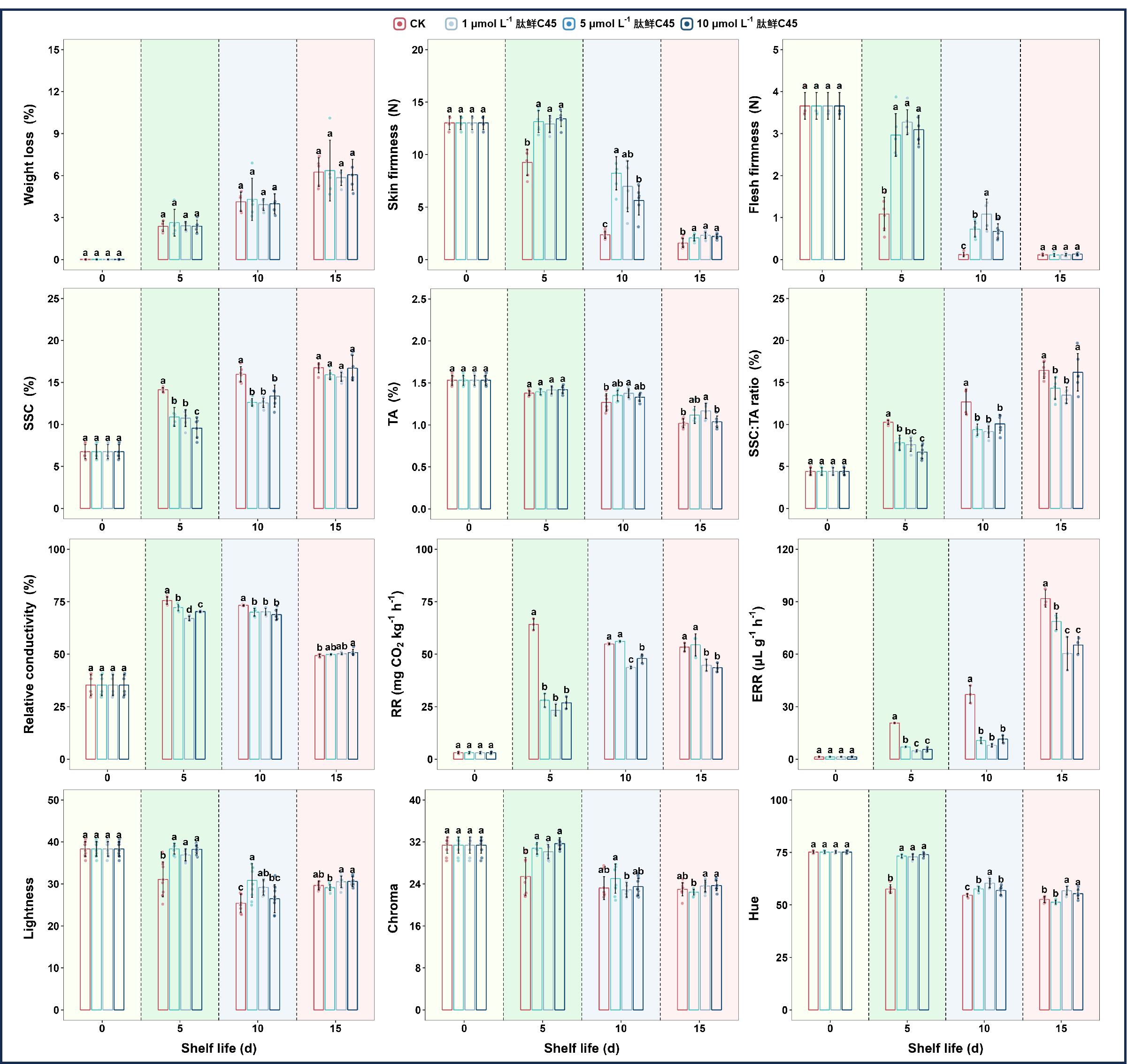
(图注:A.为果肉表型。B为果肉淀粉染色) 所有组的果实失重率都随着货架期的延长而增加。尽管在各个时间点处理之间未观察到显著差异,但肽鲜C45处理的果实在第10天和第15天的失重率最低。果皮硬度和果肉硬度都随时间的延长而下降,而肽鲜C45在第5—15天和第5—10天分别显著抑制了果皮硬度和果肉硬度的下降。不同浓度的肽鲜C45抑制了SSC的增加,在第5天和第10天与对照相比有显著差异。同时,肽鲜C45抑制了可滴定酸的降解,其中
5 µmol L⁻¹肽鲜C45在第15天效果最显著。因此,相对于对照,SSC:TA比值的增加也减少了,5 µmol
L⁻¹肽鲜C45在第15天的影响最小。肽鲜C45处理在第5天和第10天显著抑制了相对电导率。1 µmol
L⁻¹肽鲜C45处理的果实在第5天呼吸速率受到抑制,但在第10天和第15天与对照相比无显著差异;而5和10 µmol
L⁻¹肽鲜C45对呼吸速率显示出显著的抑制作用。尽管乙烯释放速率在整个货架期间增加,但所有三种浓度的肽鲜C45均显著抑制了乙烯代谢,其中5 µmol
L⁻¹肽鲜C45的作用最有效。 果肉亮度随货架期延长而下降,然后在第15天恢复;而外源肽鲜C45几乎在第5天和第10天都显著抑制了这种下降。色度和色调值都随时间下降,肽鲜C45减缓了下降,其中
5 µmol L⁻¹肽鲜C45处理在第10天和第15天的色调值最高。
图2-17 肽鲜C45施加后有关果实数据
(图注:品质变化。(A)失重百分比。(B)果皮硬度。(C)果肉硬度。(D)可溶性固形物含量。(E)可滴定酸度。(F)固酸比。(G)相对电导率。(H)呼吸速率。(I)乙烯释放速率。(J)亮度。(K)色度。)
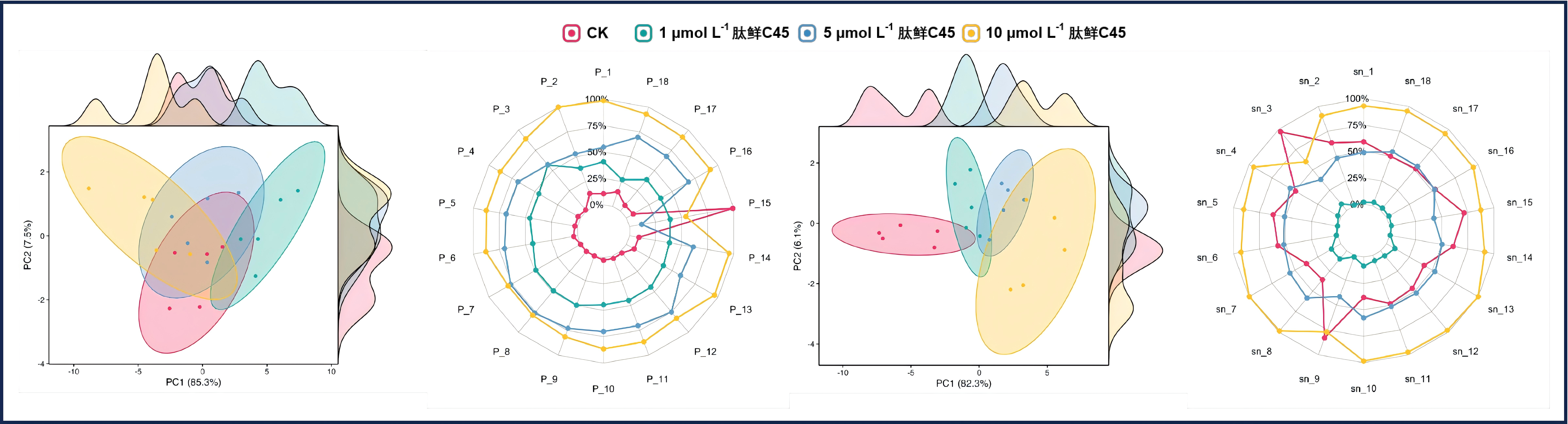
电子鼻和电子舌分析表明,肽鲜C45处理显示出一定程度的交集,并影响了果实的风味和口感。综上所述,外源肽鲜C45影响了“徐香”猕猴桃在货架期间的多个品质方面,包括形态、质地、颜色、风味、口感和生理稳定性。在所测试的浓度中,5
µmol L⁻¹肽鲜C45显示出最有效的保鲜效果,因此被选作进一步分析。
图2-18 电子鼻和电子舌分析 从左到右依次为电子鼻检测的主成分分析、电子鼻检测的雷达图、电子舌测定的主成分分析和电子舌测定的雷达图。数据以三次重复实验的平均值±标准差表示。不同小写字母表示差异显著(P
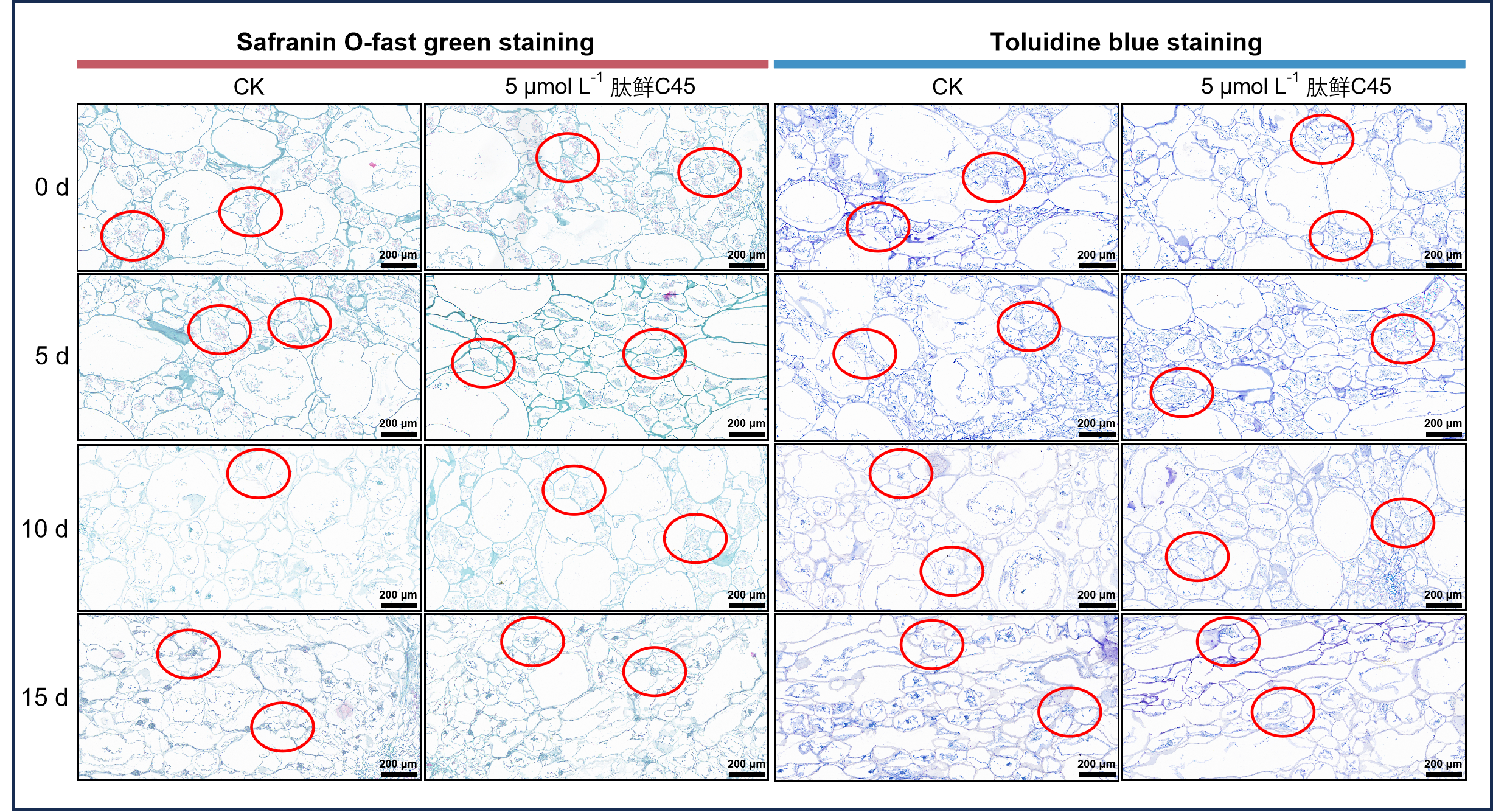
< 0.05)。 番红&固绿染色和甲苯胺蓝染色(图2-19)均显示淀粉颗粒减少、细胞壁破裂和细胞崩解,这些进一步得到扫描电子显微镜(SEM)和透射电镜(TEM)分析的证实。同样,总淀粉含量的下降也验证了这一减少。在货架期间,淀粉颗粒逐渐分化为含有大量类胡萝卜素的有色体。类胡萝卜素的积累是货架期间色调下降和黄化加剧的原因之一。淀粉和细胞壁降解是影响猕猴桃软化的关键因素,因为它们维持细胞膨压并提供结构支撑。一旦猕猴桃进入成熟过程,淀粉逐渐降解,这种结构支撑减弱,导致果肉硬度降低和软化加速。有研究揭示,抑制淀粉和细胞壁降解并维持ROS稳态可以延缓猕猴桃在常温贮藏期间的软化。5
µmol L⁻¹肽鲜C45保持了细胞结构完整性,减少了细胞劣变,并缓解了淀粉颗粒降解。 因此,肽鲜C45延缓了货架期间由后熟和衰老引起的淀粉和细胞壁降解,这也是肽鲜C45抑制软化过程和总糖升高的原因。
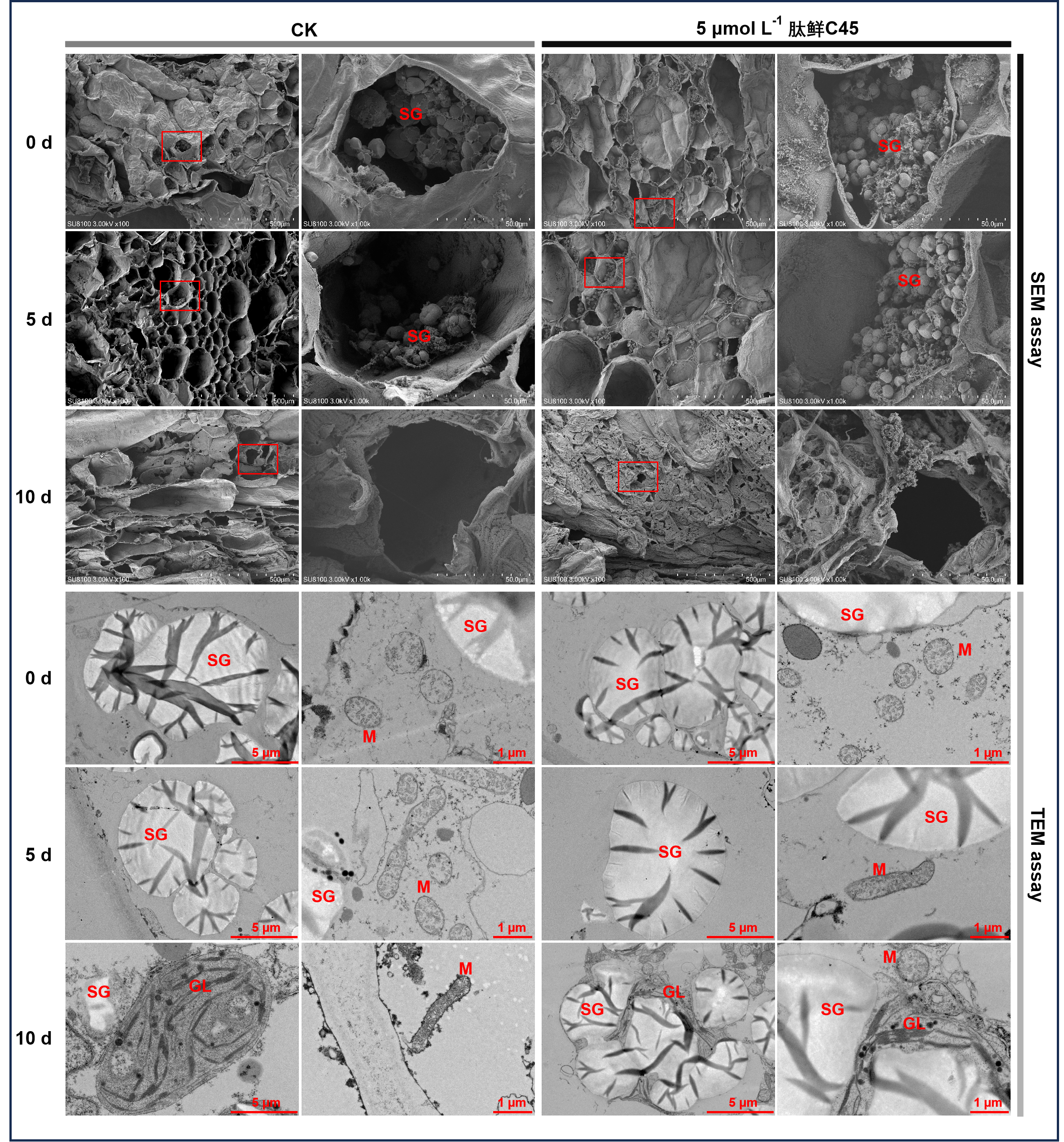
图2-19 番红&固绿染色实验结果图 从左到右依次为番红固绿染色和甲苯胺蓝染色。结果展示了5天至15天CK组(空白组)以及肽鲜C45处理组染色的变化情况。 SEM和TEM的电镜观察结果如图2-20所示。SEM分析表明,第0天的细胞结构完整,形状规则,富含淀粉颗粒。第5天,空白组果实中的大多数细胞内容物大量丢失并显示轻微变形,而肽鲜C45处理中的大部分细胞仍呈现饱满形状并含有显著的淀粉颗粒;第10天,两组的细胞都显示出明显的拉伸变形,但
5 µmol
L⁻¹肽鲜C45处理的细胞保留了一些淀粉颗粒和部分未消化的纤维状物质。TEM观察清晰地显示了淀粉颗粒和线粒体。在空白组果实中,淀粉颗粒在第5天开始碎裂并可见裂纹,第10天质体已分化为有色体。相比之下,肽鲜C45处理在第5天保持了完整的淀粉颗粒,直到第10天才出现微小裂纹。类囊体、基粒和基粒片层在肽鲜C45处理中仍然可见。第0天的线粒体主要为球形,但第5天部分线粒体延伸为杆状,表明能量需求增加。第10天,空白组中的线粒体比肽鲜C45处理中的染色更深,反映了与果实衰老相关的氧化损伤和膜降解。在货架期开始时,细胞呈现饱满且规则的形态,富含淀粉颗粒。随着货架期的进行,细胞收缩破裂,伴随细胞质泄漏和淀粉颗粒降解。相比之下,与空白组相比,5
µmol L⁻¹肽鲜C45处理保留了更多的淀粉颗粒并维持了更好的细胞完整性。 可以得出结论:外源肽鲜C45延缓了细胞结构的衰老和劣变,从而有助于保持“徐香”猕猴桃的品质并延长其货架期。
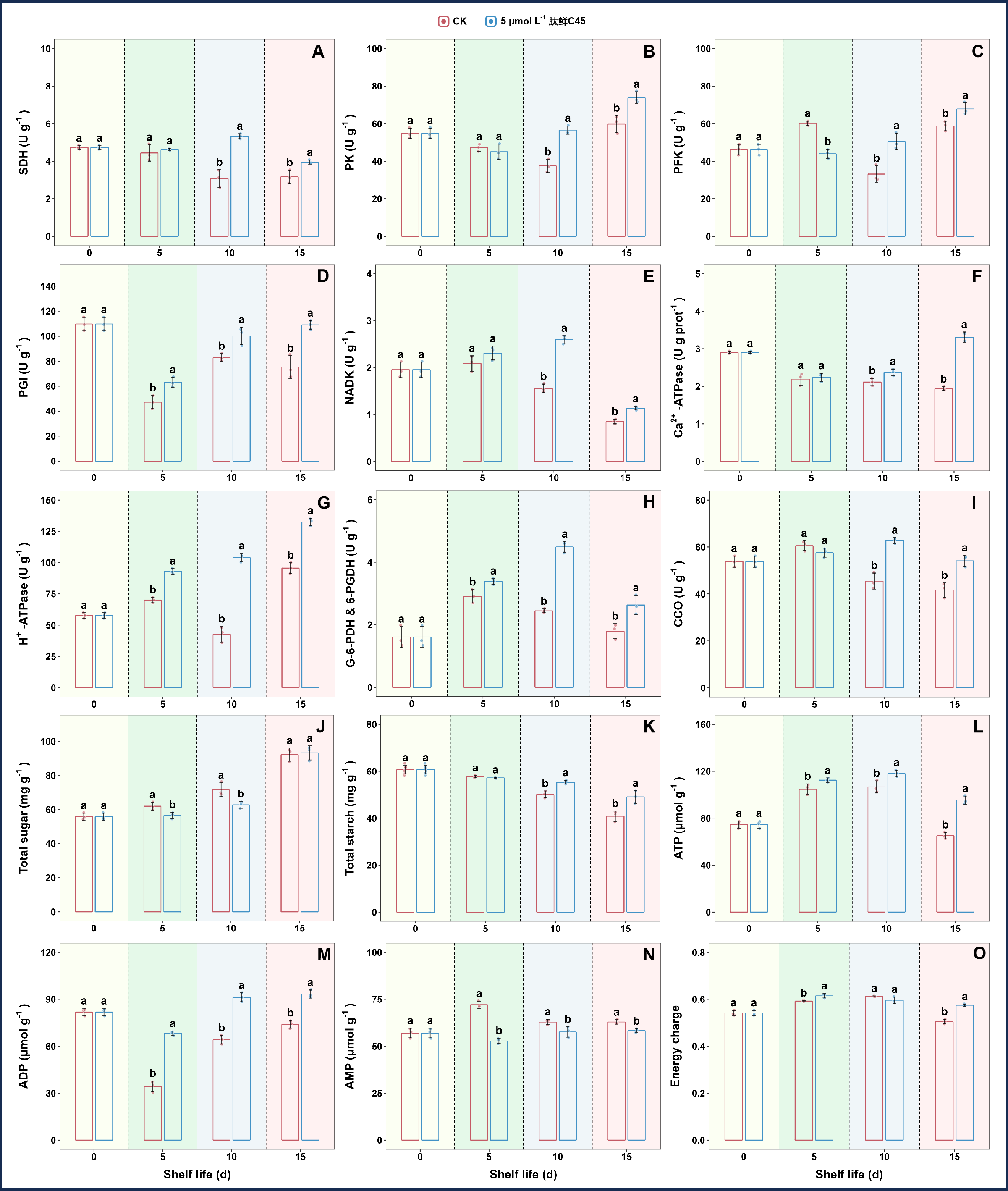
图 2-20 扫描电子显微镜以及透射电镜结果图 SEM和TEM展示了肽鲜C45处理组和对照组在0-10天的果肉细胞超微结构的结果。 与对照果实相比,肽鲜C45处理的果实显示出增强的能量代谢相关酶活性和物质含量的维持。肽鲜C45处理中
SDH、PK、PFK、NADK、Ca²⁺-ATPase 和 CCO
的活性在第10天和第15天显著高于对照;此外,在整个货架期间,肽鲜C45处理中PGI、H⁺-ATPase和G-6-PDH & 6-PGDH
的活性显著高于对照。与对照相比,肽鲜C45处理在第5—10天和第10—15天分别显著抑制了总糖的增加和总淀粉的下降。肽鲜C45处理在第5—15天显著增加了APT和ADP的含量,同时降低了AMP的含量。此外,肽鲜C45处理的能量电荷在第5天和第15天显著高于对照。肽鲜C45处理显著提升了果实中ATP、ADP含量及能量电荷水平,同时降低了AMP含量,表明细胞的能量状态更加充沛和高效。处理同时激活了糖酵解、三羧酸循环、磷酸戊糖途径和电子传递链中的多个关键酶,如琥珀酸脱氢酶、丙酮酸激酶、细胞色素c氧化酶等的活性。
此外,负责能量转运的Ca²⁺-ATPase和H⁺-ATPase活性也得到增强。小肽处理后,确保了细胞在采后阶段仍有充足的能量进行修复和维持活动,是抵抗衰老、保持品质的根本动力。SDH和6-PGDH的表达先升高后在第15天下降,与对照相比,它们在5
µmol
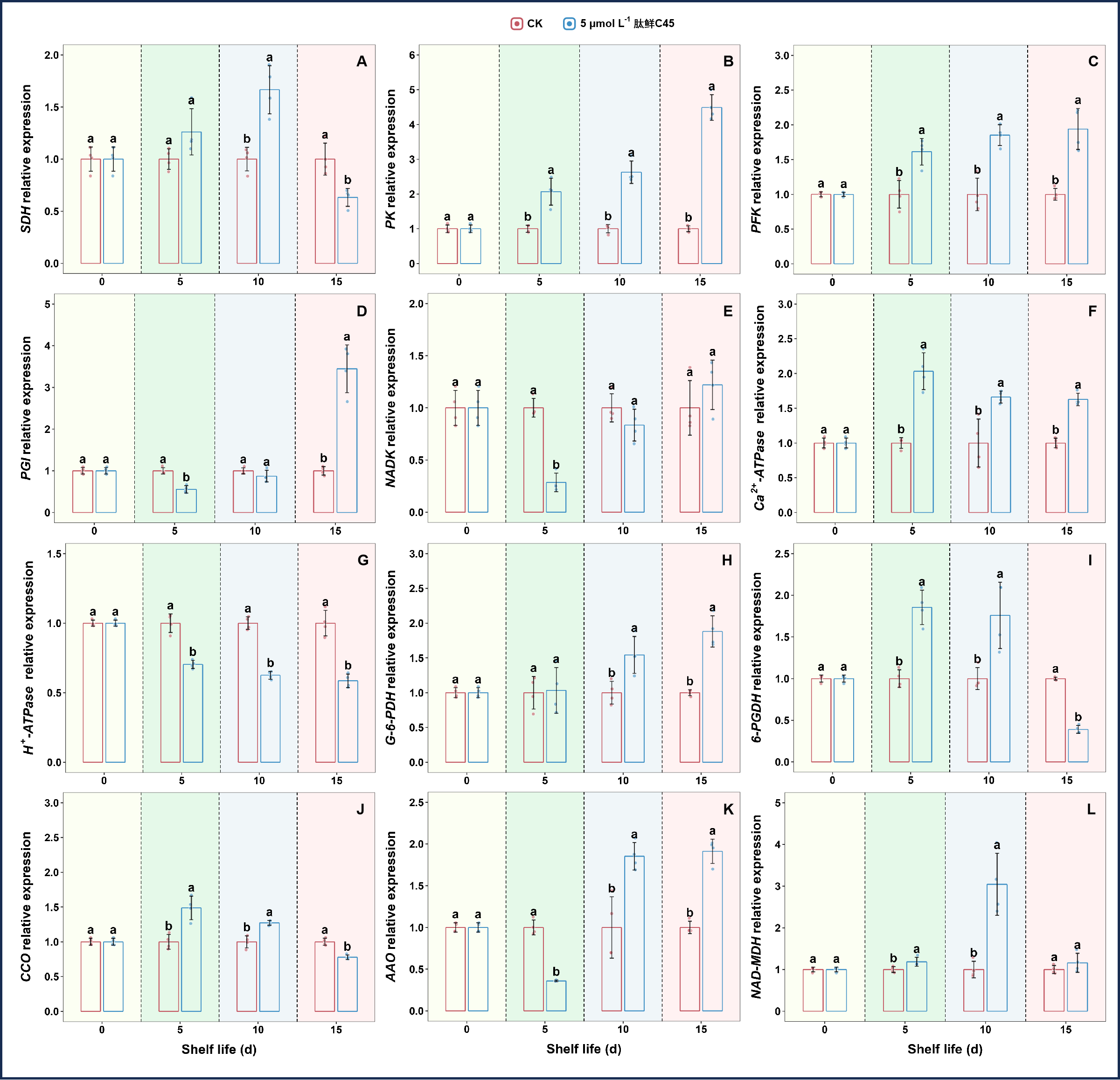
L⁻¹肽鲜C45处理下在第5天和第10天上调,但在第15天下调。外源肽鲜C45在整个货架期间几乎始终显著上调了PK、PFK、Ca²⁺-ATPase、G-6-PDH和NAD-MDH的表达水平。PGI在第5天被肽鲜C45显著下调,但在第15天显著上调。肽鲜C45处理中的NADK在第5天的表达显著低于对照,在第10天和第15天无统计学差异。在肽鲜C45处理中,H⁺-ATPase呈下降趋势,并且在货架期间始终显著低于对照。肽鲜C45处理中的
CCO
表达在第5天和第10天显著高于对照,但在第15天较低。与对照相比,AAO在第5天显著下调,但在第10天和第15天上调。因此,这些与能量代谢相关的不同表达模式解释了外源肽鲜C45减缓猕猴桃后熟、衰老和劣变的基因调控复杂性。G-6-PDH
&
6-PGDH总活性的升高表明PPP的显著激活作用。它为核酸合成提供磷酸戊糖骨架,并产生大量NADPH,为细胞抗氧化系统提供还原力。因此,它有助于维持细胞结构完整性,这一效应在肽鲜C45处理下NADK活性的增强中得到了进一步支持。NADK催化NAD⁺磷酸化为NADP⁺,从而为NADPH的产生提供前体。增加的NADPH可用性缓解了果肉细胞的氧化压力,并维持了整个货架期的细胞完整性,如微观结构的改善所证明。此外,增强的NADK活性表明外源肽鲜C45有效调节了细胞内NAD⁺/NADP⁺的平衡。
这些结果(见下图)共同证明,外源肽鲜C45通过增强关键能量代谢途径中关键酶的活性来抑制猕猴桃在货架期间的衰老。
图2-21 肽鲜C45小肽施加后能量代谢有关物质变化
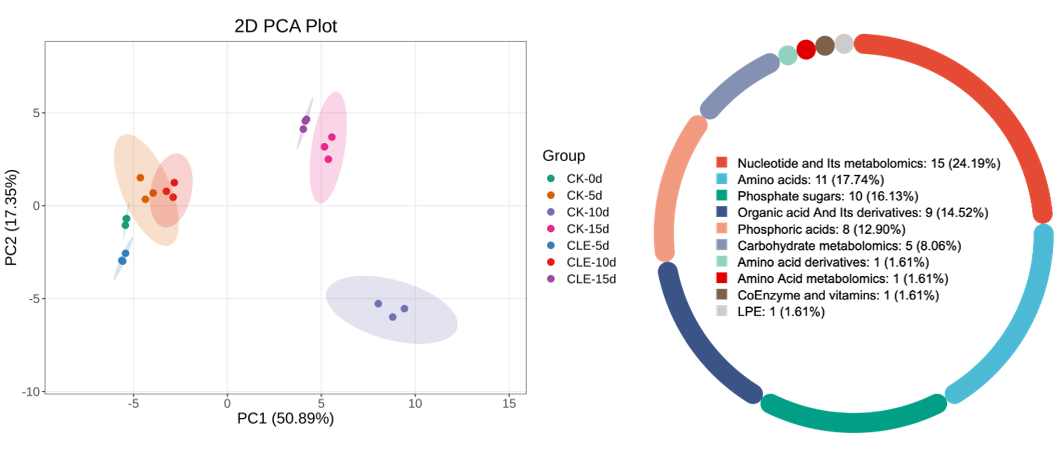
图2-22 肽鲜C45小肽施加后有关基因表达量变化 而在代谢物的变化上我们进行了PCA分析,其中表明PC1和PC2解释了总变异的68.24%。共检测到62种与能量代谢相关的代谢物,它们被分类为核苷酸及其代谢物、氨基酸、磷酸糖、有机酸及其衍生物、磷酸、碳水化合物代谢物、氨基酸衍生物、氨基酸代谢物、辅酶和维生素和LPE。每组中具体成分的变化如相关图表所示。
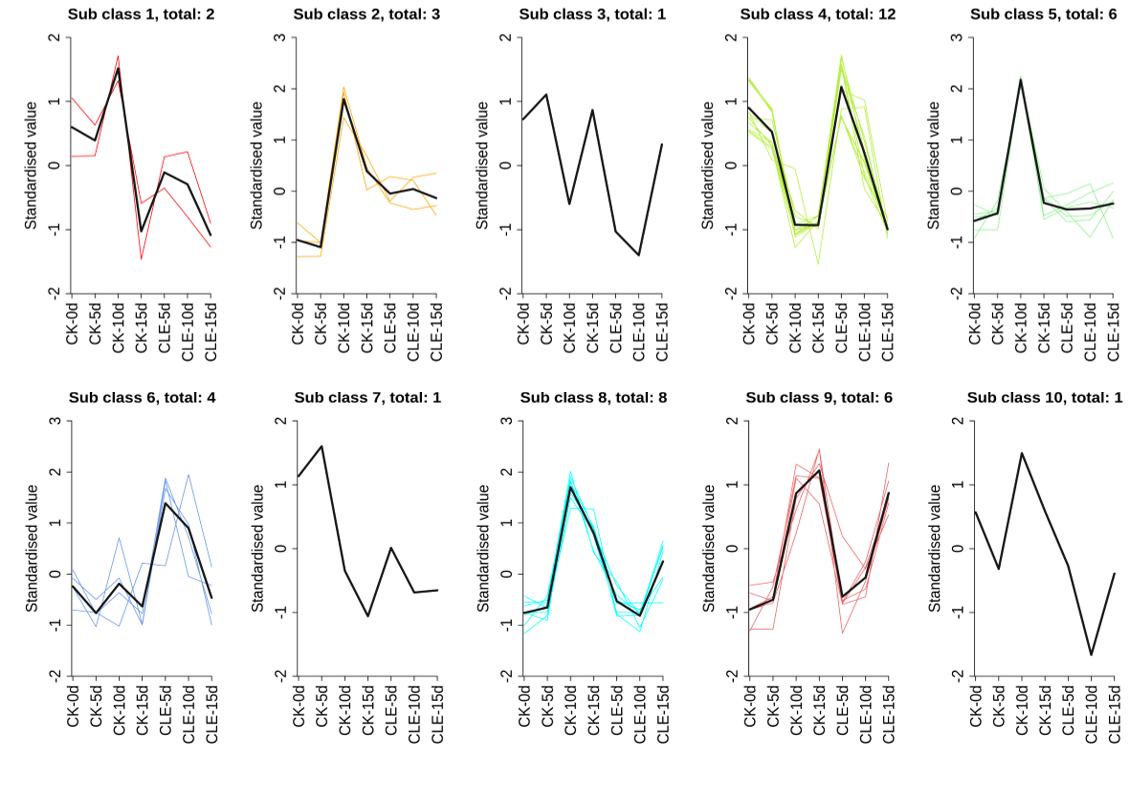
图2-23 PCA主成分分析及其注释
图2-24 Mean分析和代谢差异物亚类变化趋势 Means分析揭示了44种差异代谢物在十个不同亚类中的变化趋势。每个比较中总差异代谢物、上调差异代谢物和下调差异代谢物的数量如相关图表所示。与第0天对照相比,第5、10、15天的对照和肽鲜C45处理分别包含3和2个核心差异代谢物;然而,在第5、10、15天的肽鲜C45与对照比较中,没有核心代谢物是共有的。在第5、10、15天的肽鲜C45与对照比较中,分别有9、29和2个差异代谢物。第10天,与对照相比,肽鲜C45处理导致L-天冬氨酸水平显著升高,映射到“氨基酸的生物合成”。L-天冬氨酸是连接TCA循环和氨基酸代谢的关键节点,参与多种途径。首先,它作为丙酮酸的前体;在GNG过程中,它被转化为草酰乙酸,然后可转化为磷酸烯醇式丙酮酸进入糖酵解。这一过程促进了有机酸的积累,并有助于降低糖酸比,这与观察到的趋势一致。
其次,L-天冬氨酸参与尿素循环,与瓜氨酸结合形成精氨琥珀酸,然后转化为精氨酸和鸟氨酸。精氨酸可以进一步代谢为肌酸和一氧化氮等化合物。适量的一氧化氮可以改善猕猴桃、苹果、番茄和桃子等水果的货架品质。第三,在氨基酸代谢中,L-天冬氨酸通过转氨作用产生α-酮戊二酸,进入TCA循环。第四,L-天冬氨酸参与嘧啶代谢,通过一系列酶促反应促进DNA和RNA前体的合成,可能促进蛋白质合成和酶活性。此外,作为苹果酸-天冬氨酸穿梭的关键成分,升高的
L-天冬氨酸促进了线粒体NADH/NAD⁺与细胞质NADH/NAD⁺的细胞内氧化还原稳态。这支持了线粒体中NADH的再生,并向ETC提供电子。这些发现与肽鲜C45处理猕猴桃中CCO和Ca²⁺-ATPase的上调是一致的。
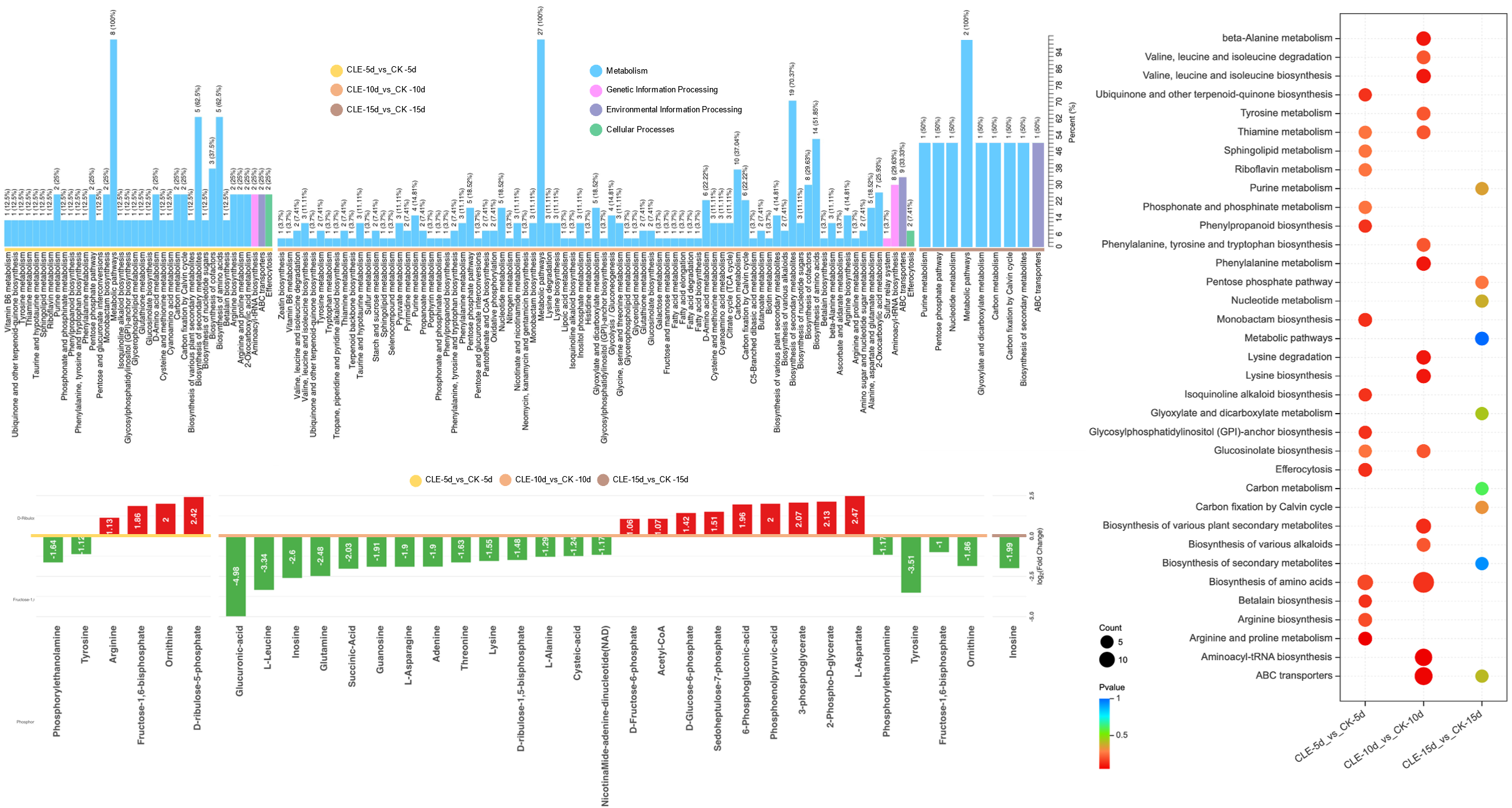
图2-25 KEGG对代谢物差异注释 KEGG
富集分析显示,这三个时间点的代谢物主要富集在38、81和9条通路中,其中“代谢途径”“次生代谢物的生物合成”和“氨基酸的生物合成”是各个阶段最主要的富集通路。KEGG
分类分析将所有通路分为四个层次,包括“代谢”“遗传信息处理”“环境信息处理”和“细胞过程”,其中“代谢”相关的通路最多。基于log2FC和KEGG图谱,最终在第5、10、15天的肽鲜C45与对照比较中分别鉴定出6、
27 和1个差异代谢物。在这方面,肽鲜C45-5d与对照-5d
的比较包括4个上调和2个下调的代谢物;肽鲜C45-10d与对照-10d的比较包括9个上调和18个下调的代谢物;而在肽鲜C45-15d
与对照-15d
的比较中,只有一种差异代谢物,即肌苷,显著下调。因此,能量代谢富集通路和差异代谢物在第10天最丰富,并且在各阶段的肽鲜C45与对照比较中存在差异,这表明能量代谢在第10天达到最高状态,这与外源肽鲜C45在维持猕猴桃采后品质中最关键的调节作用这表明能量稳态在货架期后期被破坏,伴随衰老和劣变。
综上所述,肽鲜C45通过调节多个属性,包括形态、质地、颜色、风味、口感、营养、生理稳定性和超微结构,来保持品质并延缓衰老,从而延长“徐香”猕猴桃的货架期,而能量代谢在此过程中发挥着关键作用。
针对任一目标珍稀或难繁育物种(如濒危兰花、药用红豆杉或高价值林木),本项目团队使用生物信息学的遗传基因分析,摒弃传统的愈伤组织扩繁方式,转而采用基于组学大数据的全系列小肽优化方案。
团队通过利用高通量测序技术,对目标物种进行基因组或深度转录组测序。通过生物信息学分析,系统性地鉴定基因组中编码“肽强”小肽分子的基因。通过在不同关键发育时期(如种子萌发、愈伤组织诱导、芽/根原基启动)及不同组织部位(茎尖、根尖、形成层、创伤响应区)进行转录组分析,能够精确绘制每一个小肽基因的表达图谱。
项目团队将鉴定到的小肽氨基酸序列,与拟南芥、水稻、杨树、人参等模式或近缘物种中功能已被深入研究的小肽进行多序列比对及系统进化分析。通过分析其保守功能域,我们可以依据“序列同源-功能相关”的原则,对其潜在生物学功能进行高置信度的初步预测。从根本上降低了研发的盲目性与失败率,为后续高效产品开发奠定了无可替代的数据基石。
在具体愈伤组织诱导扩繁上,以目标植物的叶片、茎段等为外植体,在培养基中添加不同小肽。通过自动化成像与图像分析,定量评估愈伤组织的诱导率、生长速率、紧实度与色泽。
图2-25 “肽强”系列小肽产品在多种植物中施加后扩繁中试
图2-26 “肽强”系列小肽产品在多种植物不定芽再生中施加后与对照组对比效果 猕猴桃溃疡病,被果农喻为“猕猴桃癌症”,是由丁香假单胞菌猕猴桃致病变种(Pseudomonas syringae pv. actinidiae,
Psa)引发的一种毁灭性细菌病害。该病害侵染枝干、叶片及花蕾,导致流脓、组织溃烂、枝梢萎蔫,严重时可直接造成整园毁灭,常年给全球猕猴桃产业带来30%至50%的巨额经济损失,已成为产业可持续发展的首要瓶颈。当前主流的防控策略高度依赖铜制剂等化学农药,不仅面临病原菌抗药性日益增强、防治效果持续下降的困境,更伴随农残超标风险、土壤微生态严重破坏及果实品质受损等一系列衍生问题。
在此背景下,本项目依托全球领先的植物小肽信号研究与合成生物学技术平台,提出了“小肽免疫激活与微生态调控”集成解决方案。本项目的核心技术在于,首次将具有完全自主知识产权的“肽壮”系列小肽及其他免疫调节肽,系统化应用于猕猴桃溃疡病的绿色防控。我们摒弃了传统农药的陈旧路径,转而通过外源施加精心设计的信号小肽,从内部调控猕猴桃植株自身强大的免疫系统与共生微生物组,从而构建起一道由内而外、多维协同的生物防御屏障。
外源施加的功能小肽作为高效的免疫激发子,能够与猕猴桃细胞膜表面特异的富含亮氨酸重复序列的受体激酶高亲和力结合。首先其能迅速诱导活性氧(ROS)的爆发,在病菌潜在的侵染点形成一道强氧化的毒性屏障,直接损伤病原菌并同步加固植物自身的细胞壁。其次,小肽信号能够系统性地启动猕猴桃自身的防御基因表达程序,显著上调包括几丁质酶、葡聚糖酶在内的多种病程相关蛋白(PR蛋白)的合成与积累。这些蛋白能直接攻击并降解Psa细菌的细胞壁,发挥直接的抗菌活性。更深层次地,该技术能智慧地调节水杨酸(SA)和茉莉酸(JA)等核心防御激素网络的平衡,使猕猴桃植株整体处于一种高度警觉的“预免疫”或“敏化”状态。在这种状态下,一旦植株检测到Psa病原菌相关的分子模式,便能做出较常规植株更为迅速、强烈的免疫响应,从而获得持久且广谱的系统性获得抗性(SAR)或诱导系统抗性(ISR)。
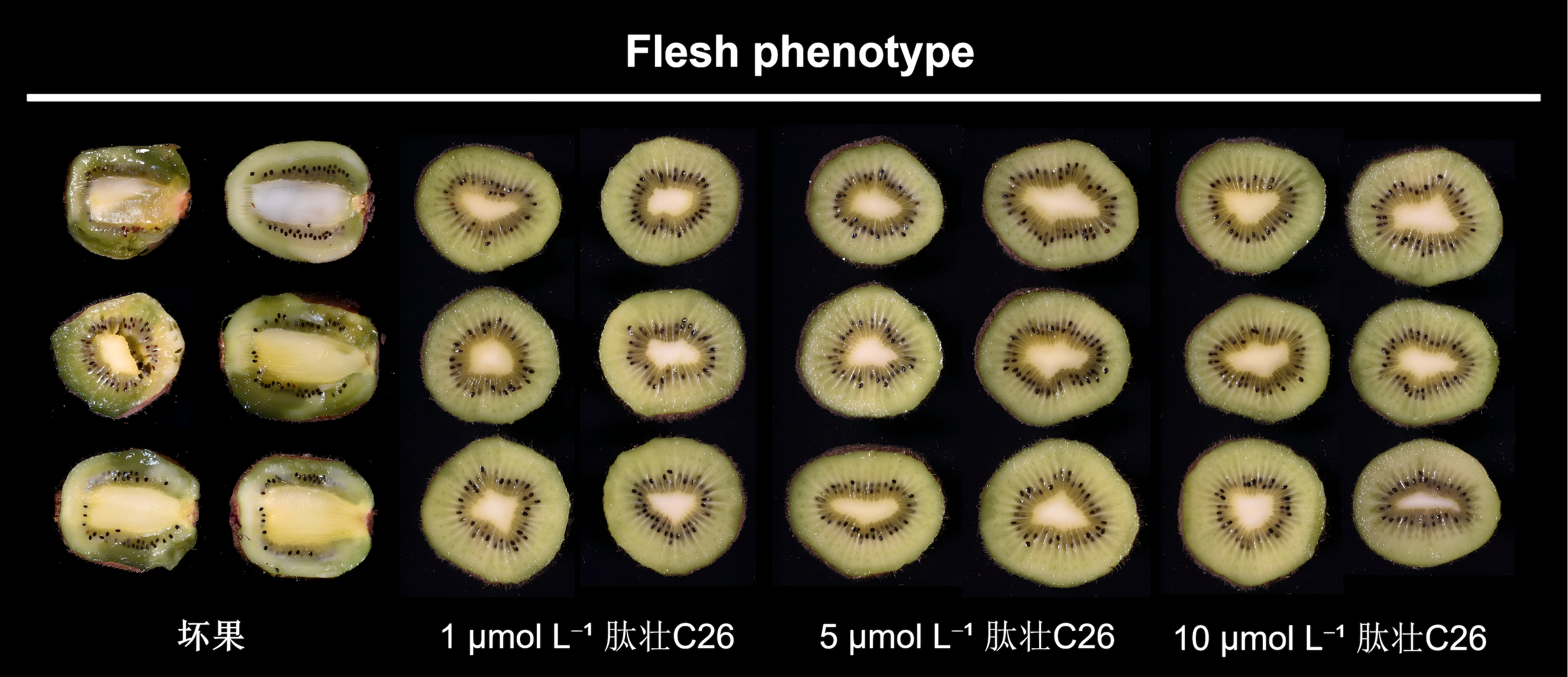
团队拍摄了3500余张从0天到15天猕猴桃的发病情况的照片,分为十余组,CK组,以及不同“肽壮”系列小肽处理后的组别,每组约80颗,共273颗发病果。其中CK组在10天和15天共发病82颗,并筛选掉三种没有保鲜效果的小肽产品。发病主要症状体现为胀气,软腐。如图2-27所示。
图2-27 肽壮C26施加后猕猴桃果实形态变化 团队在前期基础科研中发现数个精准调控气孔运动、抑制乙烯生物合成、激活内源抗氧化防御系统或延缓衰老等功效的小肽分子。因此,猜测这些小肽能够从生理与分子层面显著延缓鲜切花衰老进程。在玫瑰、香石竹等关键商业花材上的应用数据显示,团队的“肽盛”系列小肽可将瓶插寿命延长40%—135%,有效维持观赏品质,其效果超越或比肩主流进口化学保鲜剂,且具备“天然、高效、安全、可降解”的颠覆性优势。本技术是植物内源信号调控理论的成功应用,为打破进口依赖、提升我国鲜切花产业全球竞争力提供了底层技术解决方案。
图2-28 不同浓度“肽盛”类小肽作为营养液在鲜切花中的作用效果 瓶插寿命显著延长:在切花模型中,使用一定剂量“肽盛”PepBloom系列小肽配合蔗糖基质的处理方案,成功将离瓶寿命大幅度延长,能显著延长多种鲜切花花期。
观赏品质全面维持:“肽盛”PepBloom系列小肽处理后的花枝表现出更优的综合品质,花朵开放率提高,花色保持度提升,叶片黄化与脱落现象被显著抑制,得益于小肽处理维持了更高的组织含水量和鲜重。
水分平衡改善:“肽盛”PepBloom系列小肽处理能强力促进水通道蛋白基因的表达,增强花茎导水能力,使叶片相对含水量在处理后仍保持在高水平。这有效解决了鲜切花采后因导管堵塞和失水导致的“弯头”和萎蔫难题。
C25/C26基因在芽再生过程中表达模式
植物芽再生过程中C25/26多肽受体的确定

BAM1/BAM2/BAM3在植物芽再生过程中表达模式

“肽鲜”PepFresh系列小肽在保鲜功能方面上的验证
果肉外观变化统计
电子舌&电子鼻风味测试
番红固绿染色&甲苯胺蓝染色实验
扫描电子显微镜&透射电镜观察超微细胞结构
能量代谢酶活性以及基因表达量测试
代谢组学分析测试
“肽育”PepBorn系列小肽在繁育扩种方面的功效

“肽壮”PepStrong系列小肽在植物抗病中的效用
“肽盛”PepBloom系列小肽产品延缓鲜切花的衰老
